Recentemente, a Administração Estatal de Alimentos e Medicamentos da China (SFDA) aceitou oficialmente o pedido de comercialização do tafolecimabe (anticorpo monoclonal PCSK-9 que é produzido pela INNOVENT BIOLOGICS,INC), INC para o tratamento da hipercolesterolemia primária (incluindo hipercolesterolemia familiar heterozigótica e não familiar hipercolesterolemia) e dislipidemia mista.Este é o primeiro inibidor de PCSK-9 autoproduzido a se candidatar para comercialização na China.
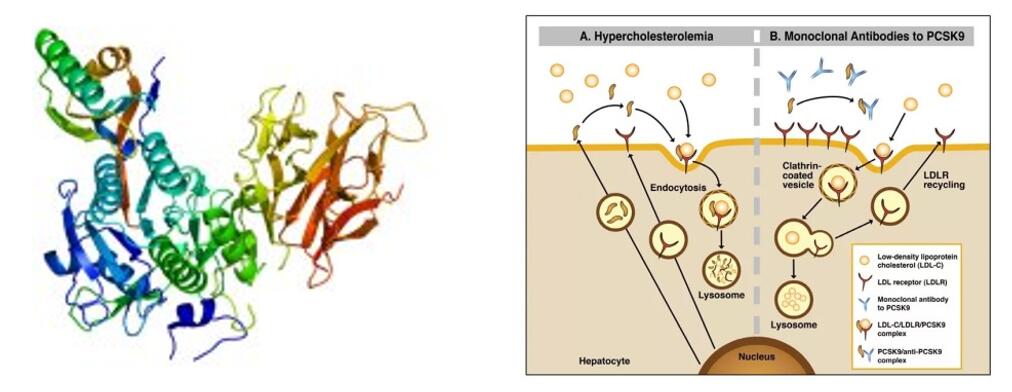
O tafolecimab é um medicamento biológico inovador desenvolvido independentemente pela INNOVENT BIOLOGICS, INC. O anticorpo monoclonal humano IgG2 liga-se especificamente à PCSK-9 para aumentar os níveis de LDLR, reduzindo a endocitose mediada por PCSK-9, aumentando assim a eliminação de LDL-C e diminuindo os níveis de LDL-C.
Nos últimos anos, a prevalência de dislipidemia aumentou significativamente na China.A prevalência de dislipidemia e hipercolesterolemia em adultos é de 40,4% e 26,3%, respectivamente.De acordo com o relatório de 2020 sobre Saúde e Doenças Cardiovasculares na China, a taxa de tratamento e controle da dislipidemia em adultos ainda está em um nível baixo, e a taxa de adesão ao LDL-C dos pacientes com dislipidemia é ainda menos satisfatória.
Anteriormente, as estatinas eram o principal tratamento para hipercolesterolemia na China, mas muitos pacientes ainda não conseguiram atingir a meta de redução do LDL-C após o tratamento.A comercialização do PCSK-9 trouxe maior eficácia aos pacientes.
A submissão do tafolecimab da INNOVENT BIOLOGICS, INC baseia-se nos resultados de três ensaios clínicos registados numa fase democrática. de administração.Os resultados do estudo CREDIT-2 foram aceitos pela Reunião Anual de 2022 do American College of Cardiology (ACC) como resumo e publicados online.
Se o pedido for aprovado, romperá o impasse do PCSK-9 impoetado, a China se tornará o quarto país a ter o PCSK-9 depois dos Estados Unidos (Amgen), França (Sanofi) e Suíça (Novartis).
Hora da postagem: 04 de julho de 2022